
안녕하세요 정리남입니다^^
이번에 이차전지'의 구조와 원리 대해 한번 살펴보려 합니다.
이번 포스팅에서는 이차전지의 의미와, 기본적인 배터리의 원리에 대해 알아보겠습니다.
연관포스팅↓↓↓
2020/09/18 이제 모든 이해 끝!!! 배터리용량, 에너지양, 에너지 밀도의 차이 정리!
2020/09/07 딱 네 가지로 끝. 리튬이온 이차전지 구조와 역할!?
2020/09/25 이차전지의 충전과 방전 원리. 이것으로 끝. (리튬이온이차전지 배터리 원리!)
2024.03.31 이차전지에서 음극재란 무엇일까?! A-Z까지 차근차근 알아보자 (대주전자재료 예상주가까지)
이차전지란 '충전이 가능한 배터리'
우리가 흔히 말하는 충전이 가능한 배터리가 바로 '이차전지'입니다. 그렇다면 일회성으로 한번 사용해서 버리는 배터리는 무엇이라할까요? 이는 '일차전지'라고 합니다. 따라서 앞으로 이차전지?라고하면 '아 충전가능한 배터리?!'라고 생각하시면 됩니다.
이 이차전지는 배터리를 구성하는 재료의 종류에 따라 납축전지, 니켈-카드뮴전지, 리튬이온전지, NaS 전지 등 여러 가지가 있습니다. 이렇가 다양한 종류가 있는 이유는, 재료의 종류에 따라 배터리의 용량이나 특징이 달라져서 사용용도에 맞게 적합한 배터리를 선택하면 되기 때문입니다.
예컨데, NaS 전지의 경우, 에너지 밀도가 높아 대용량 전력저장용으로 적합합니다. 리튬이차전지에 비해 상대적으로 저렴한 나트륨과 황을 원료를 사용하므로 가격경쟁력도 높다고 합니다. 하지만 리튬이온전지 보다는 훨씬 무거워 소형 가전에는 사용이 불가합니다. 따라서 산업용으로 주로 사용합니다. 또한 납축전지의 경우, 리튬이온전지에 비해 과충전 및 과열에 의한 폭발, 화재 등의 위험성이 현저히 적고 단가가 저렴합니다. 단, 제조단계에서부터 황산, 납 등의 원료 사용으로 환경리스크가 큰 제품이며, 배터리의 수명이 짧다는 단점이 있습니다.

예를 들어 치킨에도 정말 다양한 양념의 치킨이 있습니다. 이유는 사람마다 맛에 대한 선호도가 모두 다르기 때문입니다. 매운 것을 좋아하는 사람에게는 매운 양념의 치킨이 잘 팔릴 것이고, 짧조름한 맛을 좋아하는 사람에게는 간장 양념 치킨이 인기 있겠죠. 마찬가지로 충전이 가능한 배터리인 이차전지도 사용되는 재료에 따라 각각의 맛(=특징, 장점과 단점)이 다르기 때문에, 그 장단점을 최대한 활용할 수 있는 곳에서 알맞게 사용되는 것입니다.

배터리의 기본적인 원리 (산화와 환원 반응)
배터리의 기본 원리는 무엇일까요??
이차전지의 구조와 원리를 알아보기 전에, 일차전지의 원리를 한번 훑어보면 보다 쉽게 이해할 수 있을 것이라 생각합니다. 제가 여기저기에서 공부한 내용을 스토리라인을 입혀 한번 쉽게 설명을 해볼테니 가볍게 쭉 읽어나가 보시길 바랍니다.
배터리는 무엇일까요?
배터리는 전기를 발생시키는 것입니다.
그렇다면 전기는 어떻게 발생될까요?
전기란, 바로 전류의 흐름을 말하죠. 그런데 전류가 흐르는 것은 사실 전자가 이동하기 때문입니다. 전류는 플러스에서 마이너스로, 전자는 그 반대 방향인 마이너스에서 플러스로 흐른다는 이야기를 한번쯤은 들어보셨을 것입니다. 우리가 흔히 전기라 일컫는, 이 전류가 흐른다는 것은 사실, 어떠한 재료(=원자)에 붙어있던 전자가 어떠한 연유에서 따로 떨어져나와 한쪽방향(마이너스에서 플러스로)으로 흐른다는 것을 이야기 합니다.
(정리)
배터리가 전기를 발생시킬 수 있는 이유는 결국, '전자'를 한쪽 방향(마이너스 → 플러스)으로 흘려주기 때문이다
그런데 이 전자라는 녀석은 과연 어떻게 해서 마이너스에서 플러스라는 방향으로 '자발적으로' 흘러가는지가 궁금해 질텐데요. 이는 '산화'와 '환원' 반응과 관련되어 있습니다. 어렵지 않습니다. 계속 쭉 이어가 보겠습니다.
쉽게 말해, 산화는 '금속의 부식'과 같고, 환원은, '금속의 석출'과 같습니다.
그런데 금속의 부식은 뭔가 '분해되는 느낌'인데요, 이를 화학적으로 살펴 보면, 어떠한 금속에서 '전자'가 분리되어 빠져나오는 것을 말합니다. 이를 화학적 용어로 '산화'라고 하며, 부식이 잘 된다는 것은 '반응성이 크다'라고 할 수 있습니다. 반면 금속의 석출은 '어떠한 금속이 생성되는 것'을 의미하는데요, 이를 화학적으로 보면 , 어떠한 것(=이온)에서 '전자'가 붙어 합쳐지는 것을 말하며 이를 '환원'이라고 합니다. 금속으로 석출된다는 것은 구조적으로 완성된 안정적인 상태가 되고 싶어한다는 것과 같으므로 '반응성이 작다'라고 할 수 있습니다.

(정리)
-. 금속의 부식 = 산화 = 전자를 분리하여 내어놓다 = 반응성이 크다
-. 금속의 석출 = 환원 = 전자가 받아들이다 = 반응성이 작다
위에서 배터리에 전기가 흐르려면 전자가 마이너스에서 플러스로 이동해야한다고 했습니다.
만약에 부식되기 쉬운 즉, 전자를 분리하여 내어놓기 쉬운 A라는 금속을 (-)극으로 삼고, 전자를 받아들여 환원되려하는 B라는 금속을 (+)극으로 삼는다면! (-)극의 A금속에서 떨어져나온 전자는, 반응성이 작은 (+)극의 B라는 금속으로 이동하여 붙으려 할 것입니다. 그리고 이렇게 마이너스에서 플러스로 전자들이 계속해서 이동하면서 전류가 흐르는(=전기가 발생)게 되는 것입니다.
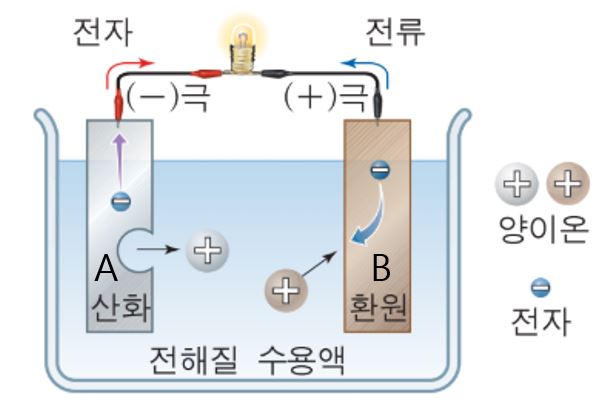
자! 그러면 기본적인 배터리의 구조를 이해할 수 있습니다.
배터리는 전기를 발생시키는 녀석인데, 이 전기는 전자의 이동이 마이너스에서 플러스로 흐를때 발생되며, 전자를 마이너스에서 플러스로 이동시키려면 반응성이 커서 산화되기 쉬운 물질을 마이너스극으로 삼고 반응성이 작아 환원되기 쉬운 물질은 플러스 극으로 삼으면 된다는 것입니다. 마이너스극에서 떨어져나온 전자가 환원되려하는 플러스극의 물질로 '자발적으로' 움직이면서 전류가 발생되기 때문입니다.
(정리)
결국, 배터리의 기본 원리는 전자를 분리하여 내어놓는 '산화'와 전자를 받아 합쳐지는 '환원' 이라는 화학 반응 때문이다. 그리고 이 배터리는 이러한 산화와 환원이라는 '화학반응'을 통해 '전기적 에너지를 발생시키는 물질'이다.
그렇다면 충전 무엇일까?
따라서 다음 포스팅으로 이어질 이차전지의 원리도 대략 짐작을 할 수 있습니다.
배터리가 배터리로서의 역할, 즉 다른 전자기기에 에너지를 공급하는 과정을 할때를 '방전'이라 하고, 그 반대의 과정이 바로 '충전'이 되는 것이죠. 바로 위에서 설명드린 원리는 '방전'과정을 말씀드렸던 것입니다. 방전할 때에는, 배터리를 구성하는 재료에서 전자가 분리되어 마이너스에서 플러스로 이동하는데 이는 물이 위에서 아래로 흐르는것과 같이 '자발적인 이동'이다 라는 것을 기억하시길 바랍니다.
그렇다면 충전은?
충전은 배터리가 방전을 시작하기 전 상태로 만들어 놓는 것이라 생각하면 되겠네요. 비디오 테입에서 되감기가 있듯이 전자가 마이너스에서 플러스로 이동하며 방전되는 상황을 되감기하듯 반대로 돌려 플러스에서 마이너스로 처음의 상태로 옮겨 놓을 수 있다면 이것이 결국 충전이 되는 것입니다.
하지만 물이 위에서 아래로 떨어지듯이 전자가 마이너스에서 플러스로 이동하는 것이 자연스러운 현상인데, 충전을 하려면 플러스에서 마이너스로 자연을 역행해야합니다. 물을 다시 아래에서 위로 올려놓아야 하는 것처럼요. 따라서 이를 위해 전원장치인 충전기의 도움을 받게되며, 충전은 방전과 다르게 '비자발적 과정'이라고 이야기 합니다.
한편, 일차전지에서는, 일단 산화되어 전자를 잃었다면 다시 환원되지 못합니다(비가역적). 하지만 이차전지는 그 구조와 재료의 특성적으로 산화와 환원 반응을 다시 일으킬 수 있습니다(가역적). 따라서 충전과 방전이 반복적으로 가능한 것입니다.
(정리)
-. 충전은 방전의 반대 메커니즘으로 전자가 비자발적으로 플러스에서 마이너스로 이동되는 것이다.
비자발적 이동을 위해 충전기와 같은 전원장치의 도움을 받는다.
-. 일차전지는 한번 산화되면 다시 환원될 수 없다. 이러한 성질을 비가역적이라 한다.
이차전지는 산화와 환원을 반복해서 일으킬 수 있다. 이를 가역적 성질이라 한다.
연관포스팅↓↓↓
2020/09/18 이제 모든 이해 끝!!! 배터리용량, 에너지양, 에너지 밀도의 차이 정리!
2020/09/07 딱 네 가지로 끝. 리튬이온 이차전지 구조와 역할!?
2020/09/25 이차전지의 충전과 방전 원리. 이것으로 끝. (리튬이온이차전지 배터리 원리!)
출처
1. https://m.blog.naver.com/hohwon/221317062190
2. http://study.zum.com/book/13414
3. https://medium.com/@youngji/%EC%A0%84%EC%A7%80-battery-%EC%9D%98-%EC%9B%90%EB%A6%AC-c209edc1ee53
4. https://www.industrynews.co.kr/news/articleView.html?idxno=34056
5. https://www.samsungsdi.co.kr/column/all/detail/55269.html
6. https://2sideline.tistory.com/entry/NaS-%EC%A0%84%EC%A7%80-%EB%82%98%ED%8A%B8%EB%A5%A8-%ED%99%A9-%EC%A0%84%EC%A7%80-%EC%A0%95%EC%9D%98-%EB%B0%8F-%EC%8B%9C%EC%9E%A5
7. https://blog.naver.com/tjdxor159/222038098431
**유의사항**
이 블로그의 모든 포스팅은 '개인적인 공부를 겸하는 글에 불과'합니다. 작성된 내용은 '저의 개인적인 의견'이 포함되어 있으며 '사실과 다를 수' 있습니다. 따라서 기타 정보들과 비교해 보시고 본 포스팅은 '참고용'으로만 봐주시길 바랍니다. 해당 정보로 인해 발생되는 어떠한 불이익에 대해서도 책임도 지지 않는다는 점 유념해주세요!
'기술,산업' 카테고리의 다른 글
| 이제 모든 이해 끝!!! 배터리용량, 에너지양, 에너지 밀도의 차이 정리! (7) | 2020.09.18 |
|---|---|
| 딱 네 가지로 끝. 리튬이온 이차전지 구조와 역할!? (0) | 2020.09.07 |
| 건설에서 턴키 방식 계약 Turn key 란 무엇일까? 장점과 단점은? (0) | 2020.01.15 |
| 정유에서의 경질유와 중질유의 의미. API도 비중의 개념과 함께 이해해보자 (1) | 2020.01.05 |
| FEED와 EPC 무엇일까? 플랜트 엔지니어링의 절차를 알아보자! (0) | 2020.01.05 |